
处方药 日本
| 通用名称 | 卫克泰 |
| 药品规格 | 6mg 4mg 2mg 8mg 10mg |
| 生产企业 | 日本Eisai |
| 功能主治 | 成人和12岁及以上儿童癫痫部分发作患者(伴有或不伴有继发性全面发作)的加用治疗。 |
注:呲仑帕奈 perampanel Fycompa为处方药物,外包装仅供参考,需在医生指导下使用,用药前请仔细阅读药品说明书,了解用法用量、禁忌症及不良反应。
【药品说明书】
适应症
成人和12岁及以上儿童癫痫部分性发作患者(伴或不伴继发性全面性癫痫发作)的加用治疗。
用法用量
成人和青少年 必须按服患者个体应答滴定吡仑帕奈剂量,以优化疗效与耐受性的平衡。 本品应在睡前口服,每日一次。 部分性癫痛发作 研究表明,吡仑帕奈4 mg日至12 mg/日可有效治疗部分性癫痫发作,本品治疗起始剂量为2 mg/日。可根据临床应答及耐受性以每次2mg的增量来增加剂量,每次加量间隔至少1周或2周(具体间隔按照下述合并药物半衰期考虑),使维持剂量达到4 mg/日至8 mg日。 根据8mg/日剂量时个体临床应答及耐受性情况,剂量最高可增加至12mg/日,每次加量间隔至少1周或2周(具体闻隔按照下述合并药物半衰期考虑),每次增量为2mg。 如患者合并使用的药物不缩短本品的半衰期,则本品每次加量滴定闻隔至少2周。如患者合并使用的药物会缩短本品的半衰期,则间隔至少1周。 停药 建议逐步减量至停药使癫痫复发的可能性降到最低。但是,由于吡仑帕奈的半衰期较长且停药后血浆浓度下降缓慢,因此在必要时可立即停药。 漏服 单次漏服:由于吡仑帕奈半衰期长,患者应等待至预定时间服用下一次剂量。 如果多次漏服,但持续时间小于5个半衰期(未服用本品代谢诱导性抗癫痫药物的患者为3周,服用本品代谢诱导性抗癫痫药物的患者为1周),应考虑从末次剂量水平起重新开始治疗。 如果患者持续停用本品的时间超过5个半衰期,建议应遵循上文给出的推荐初始剂量重新滴定。 老年人(65岁及以上) 吡仑帕奈临床研究未纳入足够数悬年龄之65岁的受试者,不能确定该人群对药物的应答是否与年轻受试者不同,对905名接受本品治疗的老年受试者的安全进行(在非癫痫适应症中进行的双官研究),结果显示无年龄相关的安全性特征差异,分析结果表明老年人无需调整剂量,考虑到接受多药治疗的患者可能发生药物相互作用,因此本品慎用于老年患者。 肾脏损害 吡仑帕奈用于轻度肾脏损害患者时,不需调整剂量。不建议将本品用于中度或重度肾脏损害患者。 肝脏损害 吡仑帕奈用于轻度和中度肝脏损害患者时,剂量增加应基于临床应答及耐受性。对于轻度或中度肝脏损害患者,可按2 mg/日剂量开始滴定。这根据患者耐受性和有效性,以2 mg剂量,每2周或更长时间上调滴定剂量。 轻度和中度肝脏损害患者,本品剂量不应超过8 mg/日. 不建议用于重度肝脏损害患者。 儿料人群 尚未确定吡合帕泰用于12岁以下儿童的安全性和疗效。 用法 每日1次:睡前口服,空腹或与食物同服均可。本品应整片吞服,切勿咀嚼、压碎或掰开。由于药片无刻痕,所以本品不能均匀掰开。
成份
主要成份:吡仑帕奈 化学名称:5‘-(2-氰基苯基)-1‘-苯基-2,3-联吡啶基-6‘(1‘H)-酮水合物(3/4) 分子式:C23H15N3O • 3/4H2O 分子量:362.90
性状
本品为橙色(2mg规格)的薄膜衣片,除去包衣后显白色或类白色。
不良反应
头晕、嗜睡、头痛、疲劳、易怒、恶心、跌倒
禁忌
对本品的活性成分或乳糖过敏者禁用。 因本品含乳糖,有罕见的遗传性半乳糖不耐受问题、Lapp乳糖酶缺乏症或葡萄糖-半乳糖棘手不良的患者不应使用本品。
注意事项
自杀观念 曾在因多种适应症接受癫痫药治疗的患者汇总报告自杀观念和行为,对于抗癫痫药随机、安慰剂对照试验所做的一项荟萃分析也显示,自杀观念和自杀行为的风险有小幅增加。上述风险产生的机制不详,但是现在数据不能排除使用吡仑帕奈时上述风险增加的可能性。 因此,应对患者进行自杀观念和自杀行为迹象的检测,同时应考虑给予恰当的治疗。应告知患者(及患者的护理者)如出现自杀观念或自杀行为迹象应就医。
药物相互作用
奈玛特韦和利托那韦均为 CYP3A 的底物,任何影响CYP3A 代谢酶活性的药物都会改变奈玛特韦和利托那韦的代谢,进而影响其有效性和安全性。此外,利托那韦本身是不可逆的 CYP3A 的强效抑制剂,可以升高其他 CYP3A 底物的血药浓度,进而增强联用药物的疗效或增加不良反应的发生风险。因此,NMV-r 不得与高度依赖CYP3A 清除且其血浆浓度升高会导致严重和/或危及生命的不良反应的药物联用。不得与强效 CYP3A 诱导剂联用,否则会导致 NMV-r 血浆浓度显著降低,可能引起病毒学应答丧失和潜在耐药性
药理作用
全球数据 已在健康成人受试者(年龄18岁至79岁)、成人和青少年部分性癫痫发作和原发性全面性强直阵挛发作患者、成人帕金森病患者、成人糖尿病神经病变患者、成人多发性硬化症患者以及肝脏损害受试者中研究了吡仑帕奈的药代动力学。 吸收 口服后,本品容易被吸收,未见明显首过代谢的证据。在极入高脂肪膳食的同时给予本品,对本品Cmax或总暴露量(AUCo-inf) 没有影响,与空腹条件下相比,进食状态下达峰时间(tmax) 延迟约1小时。 分布 体外研究数据显示,大约95%的吡仑帕奈与血浆蛋白相结合。 体外研究表明,吡仑帕奈并不是下列物质的底物或明显抑制剂,有机阴离子转运多肽(OATP) 1B1和1B3、有机阴离子转运蛋白(OAT) 1、2、3和4、有机阳离子转运蛋白(OCT) 1、2和3以及外排型转运体P-糖蛋白和乳腺癌耐药蛋白(BCRP)。
贮藏
不超过30°C密闭保存。
【适应症】
成人和12岁及以上儿童癫痫部分性发作患者(伴或不伴继发性全面性癫痫发作)的加用治疗。
【副作用】
头晕、嗜睡、头痛、疲劳、易怒、恶心、跌倒
【用法用量】
成人和青少年 必须按服患者个体应答滴定吡仑帕奈剂量,以优化疗效与耐受性的平衡。 本品应在睡前口服,每日一次。 部分性癫痛发作 研究表明,吡仑帕奈4 mg日至12 mg/日可有效治疗部分性癫痫发作,本品治疗起始剂量为2 mg/日。可根据临床应答及耐受性以每次2mg的增量来增加剂量,每次加量间隔至少1周或2周(具体间隔按照下述合并药物半衰期考虑),使维持剂量达到4 mg/日至8 mg日。 根据8mg/日剂量时个体临床应答及耐受性情况,剂量最高可增加至12mg/日,每次加量间隔至少1周或2周(具体闻隔按照下述合并药物半衰期考虑),每次增量为2mg。 如患者合并使用的药物不缩短本品的半衰期,则本品每次加量滴定闻隔至少2周。如患者合并使用的药物会缩短本品的半衰期,则间隔至少1周。 停药 建议逐步减量至停药使癫痫复发的可能性降到最低。但是,由于吡仑帕奈的半衰期较长且停药后血浆浓度下降缓慢,因此在必要时可立即停药。 漏服 单次漏服:由于吡仑帕奈半衰期长,患者应等待至预定时间服用下一次剂量。 如果多次漏服,但持续时间小于5个半衰期(未服用本品代谢诱导性抗癫痫药物的患者为3周,服用本品代谢诱导性抗癫痫药物的患者为1周),应考虑从末次剂量水平起重新开始治疗。 如果患者持续停用本品的时间超过5个半衰期,建议应遵循上文给出的推荐初始剂量重新滴定。 老年人(65岁及以上) 吡仑帕奈临床研究未纳入足够数悬年龄之65岁的受试者,不能确定该人群对药物的应答是否与年轻受试者不同,对905名接受本品治疗的老年受试者的安全进行(在非癫痫适应症中进行的双官研究),结果显示无年龄相关的安全性特征差异,分析结果表明老年人无需调整剂量,考虑到接受多药治疗的患者可能发生药物相互作用,因此本品慎用于老年患者。 肾脏损害 吡仑帕奈用于轻度肾脏损害患者时,不需调整剂量。不建议将本品用于中度或重度肾脏损害患者。 肝脏损害 吡仑帕奈用于轻度和中度肝脏损害患者时,剂量增加应基于临床应答及耐受性。对于轻度或中度肝脏损害患者,可按2 mg/日剂量开始滴定。这根据患者耐受性和有效性,以2 mg剂量,每2周或更长时间上调滴定剂量。 轻度和中度肝脏损害患者,本品剂量不应超过8 mg/日. 不建议用于重度肝脏损害患者。 儿料人群 尚未确定吡合帕泰用于12岁以下儿童的安全性和疗效。 用法 每日1次:睡前口服,空腹或与食物同服均可。本品应整片吞服,切勿咀嚼、压碎或掰开。由于药片无刻痕,所以本品不能均匀掰开。
【注意事项】
自杀观念 曾在因多种适应症接受癫痫药治疗的患者汇总报告自杀观念和行为,对于抗癫痫药随机、安慰剂对照试验所做的一项荟萃分析也显示,自杀观念和自杀行为的风险有小幅增加。上述风险产生的机制不详,但是现在数据不能排除使用吡仑帕奈时上述风险增加的可能性。 因此,应对患者进行自杀观念和自杀行为迹象的检测,同时应考虑给予恰当的治疗。应告知患者(及患者的护理者)如出现自杀观念或自杀行为迹象应就医。
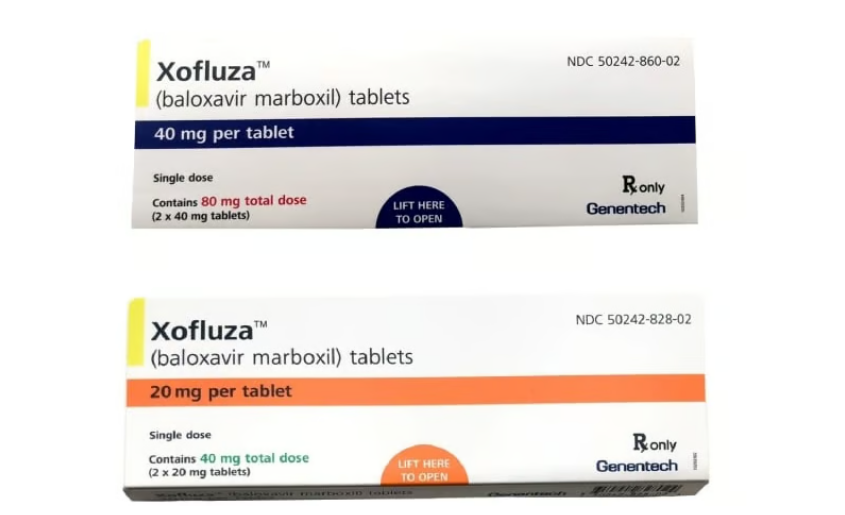
罗氏已签署一项自愿许可协议,允许仿制药企在129个发展中国家复制其畅销流感抗病毒药物Xofluza(巴洛沙韦马布酯)。药品专利池(MPP)在5月18日发布的公告...

去年秋天 III 期临床数据亮眼之后,阿斯利康对 CinCor Pharma 及其醛固酮合酶抑制剂(ASI)baxdrostat 的押注持续获得回报。FDA 已...
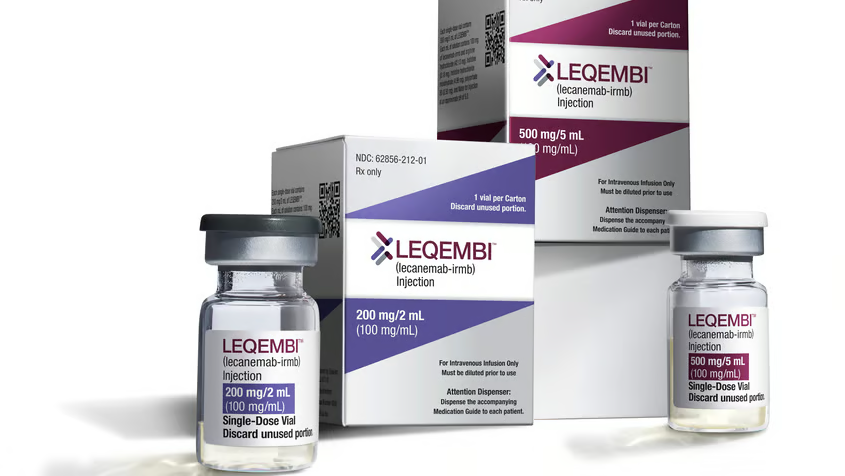
如今,卫材在 5 月 15 日发布的全年财报演示中表示,预计 2026 财年 Leqembi 的收入将达到 1435 亿日元(约合 9.046 亿美元)。大部分...

仿制药巨头太阳制药(Sun Pharma)正在美国召回一批化疗药物,颗粒物污染问题再次出现在 FDA 的召回名单上。 根据 FDA 网站上发布的公告,太阳制药此...

在抗癌免疫疗法Unloxcyt获得FDA批准三个月后,Checkpoint Therapeutics找到了买家。 两家公司周日宣布,太阳制药已同意以3.55亿美...
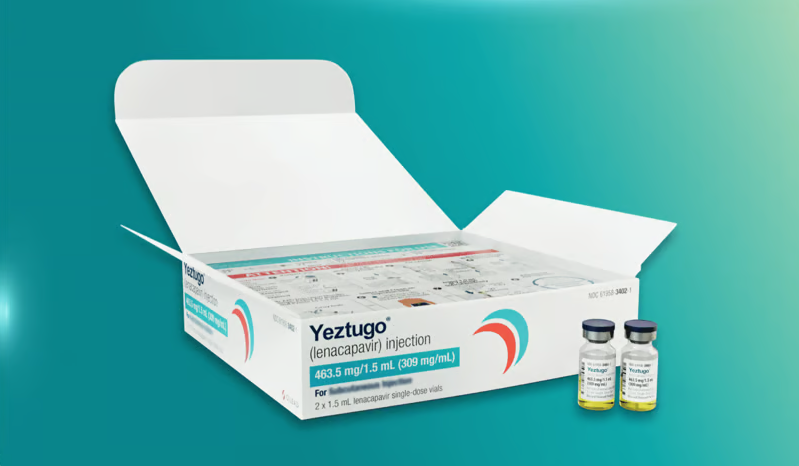
从长达17年的研发周期到最终商业化上市,生产一直深深植根于Yeztugo的DNA之中。对于这款每年只需注射两次的暴露前预防(PrEP)药物——吉利德科学将其定位...






