从长达17年的研发周期到最终商业化上市,生产一直深深植根于Yeztugo的DNA之中。对于这款每年只需注射两次的暴露前预防(PrEP)药物——吉利德科学将其定位为终结艾滋病疫情的关键工具之一——“生产即可及”。
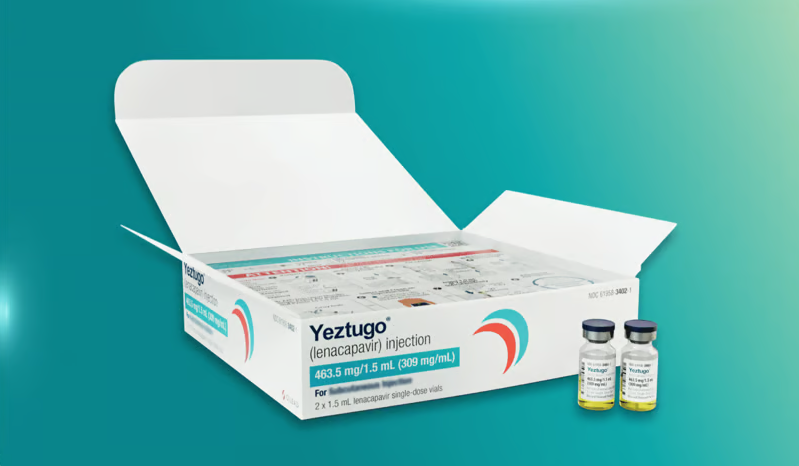
这一观点来自吉利德药物开发与制造执行副总裁马思敏博士。她近日在接受采访时表示,正是基于对可及性的长期考量,以及Yeztugo的有效成分来那卡帕韦(lenacapavir)这一复杂化合物,吉利德“从一开始”就将工艺开发和规模化生产的考量融入到了研发工作之中。
去年6月,Yeztugo走过了漫长的审批之路,终于获得美国FDA批准,成为首个每年仅需注射两次的HIV预防选项。当时,吉利德首席执行官Daniel O'Day称赞该药是“我们这个时代最重要的科学突破之一”,并强调借助Yeztugo“真正有机会帮助终结艾滋病疫情”。
此后,该药物也获得了欧盟的批准。与此同时,吉利德正在多个大洲推进注册工作,并在部分中低收入国家寻求加速审评。吉利德已经通过免版税的许可协议与六家仿制药制造商合作,开辟了额外的可及渠道。
在此期间,吉利德还与全球抗击艾滋病、结核病和疟疾基金合作,承诺在三年内提供足以覆盖200万人的Yeztugo剂量,主要面向低收入和中低收入国家。与此同时,其仿制药合作伙伴正在努力实现生产上线——马思敏预计这一时间点大约在2027年。吉利德已承诺通过全球基金以非营利价格提供这些剂量。
此外,在自己的生产网络内,吉利德正在位于加利福尼亚州拉文市的无菌产品生产基地进行扩建,以支持来那卡帕韦的生产。该基地于2017年启用。
马思敏表示,吉利德很早就启动了Yeztugo的可及性工作。在2024年来那卡帕韦在HIV预防试验中展现出令人印象深刻的疗效后不久,公司就着手对供应链规模化进行重点攻关。
她补充说,这一过程的一个关键环节是在Yeztugo获得美国FDA批准之前,就与六家免版税合作伙伴——Dr. Reddy's Laboratories、Emcure、Eva Pharma、Ferozsons Laboratories、Hetero以及Viatris子公司Mylan——启动了技术转移。她表示,广泛的药物可及性对于该药物对艾滋病疫情产生有意义的影响是必不可少的。
马思敏表示,她为自己团队提前落实来那卡帕韦可及性方面的工作感到“无比自豪”,并指出吉利德于去年6月获得该药在美国的批准,并在大约六个月的“前所未有”的时间窗口内,成功向撒哈拉以南非洲的两个国家交付了剂量。
她还补充说,吉利德仍“完全按计划”推进,将以非营利价格交付其余承诺的剂量。