
处方药 老挝
| 通用名称 | 来那卡帕韦、来那帕韦纳、Lenacapavir、ALI-LENA |
| 药品规格 | 300mg*5片;463.5mg/1.5mL/瓶*2瓶 |
| 生产企业 | 老挝联合制药 |
| 功能主治 | 该药物主要用于与其他抗反转录病毒药物联合使用,治疗当前治疗方案无法实现病毒学抑制的多重耐药1型人类免疫缺陷病毒(HIV-1)感染的成人患者。 |
注:来那帕韦Lenacapavir为处方药物,外包装仅供参考,需在医生指导下使用,用药前请仔细阅读药品说明书,了解用法用量、禁忌症及不良反应。
【药品说明书】
来那帕韦(Lenacapavir)Sunlenca是一种新型抗病毒药物,主要用于治疗HIV感染。它属于衣壳抑制剂,通过干扰病毒衣壳结构抑制病毒复制,适用于多重耐药HIV患者的联合治疗。该药为处方药,需严格尊医嘱使用。
【生产厂家】美国吉利德公司 GileadSciences,Inc.
【商标】Sunlenca
【通用名】Lenacapavir
【中文名】来那卡帕韦、利那卡帕韦
【规格】
片剂为米色胶囊状薄膜包衣片:规格一:4片/泡罩包装;规格二:5片/泡罩包装。
注射剂试剂盒包含:一、2个单剂量小瓶,每瓶足以抽出463.5mg/1.5mL(309mg/mL) Lenacapavir;二、2个药瓶接入装置、2个一次性注射器和2个用于皮下注射的注射安全针(22号,½英寸)。
【存储】
储存在20°C–25°C(68°F–77°F)温度下,允许波动范围为15°C–30°C(59°F–86°F)。片剂仅在原装泡罩包装中分装和储存。将小瓶保存在原纸盒中,直至准备注射前,以防止光线照射。将溶液抽入注射器后,应尽快进行注射。丢弃溶液中任何未使用的部分。
【来那帕韦(Lenacapavir)Sunlenca适应症和用法】
来那帕韦(Lenacapavir)Sunlenca,一种人类免疫缺陷病毒1型(HIV-1)衣壳抑制剂,与其他抗逆转录病毒药物联合使用,用于治疗因耐药、不耐受或安全性考虑而导致当前抗逆转录病毒治疗失败且具有大量治疗经验的多药耐药HIV-1感染成人的HIV-1感染。
【来那帕韦(Lenacapavir)Sunlenca剂量和给药】
推荐剂量——从两种选择中的一种开始,然后每6个月维持给药一次。服用片剂时可不考虑食物。
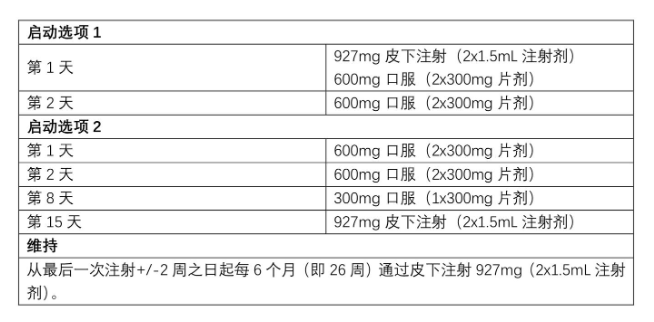
错过剂量:如果自上次注射后超过28周且临床上适合继续使用Sunlenca,则使用选项1或选项2从第1天重新开始。
完整剂量需要两次1.5 mL 皮下注射。
【来那帕韦(Lenacapavir)Sunlenca剂型和规格】
片剂:300mg。
注射剂:463.5mg/1.5mL(309mg/mL)在单剂量小瓶中。
【来那帕韦(Lenacapavir)Sunlenca禁忌症】
强CYP3A诱导剂禁止来那帕韦(Lenacapavir)Sunlenca联合给药。
【来那帕韦(Lenacapavir)Sunlenca警告和注意事项】
免疫重建综合征:可能需要进一步评估和治疗。
lenacapavir的残留浓度可能会在体循环中保留长达12个月或更长时间。就给药方案向患者提供建议;不依从性可能导致病毒学应答丧失和耐药性的进展。
在来那帕韦(Lenacapavir)Sunlenca最后一次皮下给药后9个月内开始,可能会增加对主要由CYP3A代谢的药物的暴露和不良反应的风险。
如果停药,尽可能在最后一次注射来那帕韦(Lenacapavir)Sunlenca后28周内启动替代的、完全抑制性抗逆转录病毒治疗方案。如果发生病毒学失败,请尽可能改用替代方案。
可能会发生注射部位反应,结节和硬结可能会持续存在。
【来那帕韦(Lenacapavir)Sunlenca不良反应】
最常见的不良反应(发生率大于或等于3%,所有级别)是恶心和注射部位反应。
【来那帕韦(Lenacapavir)Sunlenca药物相互作用】
在治疗前和治疗期间,请查阅完整处方信息,了解重要的药物相互作用。
【来那帕韦(Lenacapavir)Sunlenca在特定人群中使用】
哺乳:应指导感染HIV的患者不要母乳喂养,因为有可能传播HIV。
一、作用机制
靶向衣壳蛋白: 通过结合HIV衣壳蛋白,破坏其正常组装和分解过程,阻断病毒生命周期。长效作用:皮下注射剂型可实现半年一次的长效治疗,提高用药依从性。
二、适应症
用于成人HIV-1感染,尤其对现有抗逆转录药物耐药或治疗失败的患者。
需与其他抗病毒药物联用,避免单独使用导致耐药性。
三、用法与用量
注射剂: 通常每6个月皮下注射一次,具体剂量由医生根据患者情况调整。
片剂 : 每次600mg,使用时间遵循医生指导安排。
四、常见副作用
1.注射部位反应(疼痛、红肿)。
2.头痛、腹泻、恶心等胃肠道症状。
五、注意事项
1.耐药风险:单独使用易引发耐药,必须联合其他抗病毒药物。
2.禁忌人群:对成分过敏者、严重肝肾功能不全者慎用;妊娠期和哺乳期需评估风险。
3.药物相互作用:可能与部分抗病毒药、肝酶诱导剂存在相互作用,需告知医生用药史。
【适应症】
来那帕韦(Lenacapavir)Sunlenca,一种人类免疫缺陷病毒1型(HIV-1)衣壳抑制剂,与其他抗逆转录病毒药物联合使用,用于治疗因耐药、不耐受或安全性考虑而导致当前抗逆转录病毒治疗失败且具有大量治疗经验的多药耐药HIV-1感染成人的HIV-1感染。
【副作用】
最常见的不良反应(发生率大于或等于3%,所有级别)是恶心和注射部位反应。
【用法用量】
推荐剂量——从两种选择中的一种开始,然后每6个月维持给药一次。服用片剂时可不考虑食物。
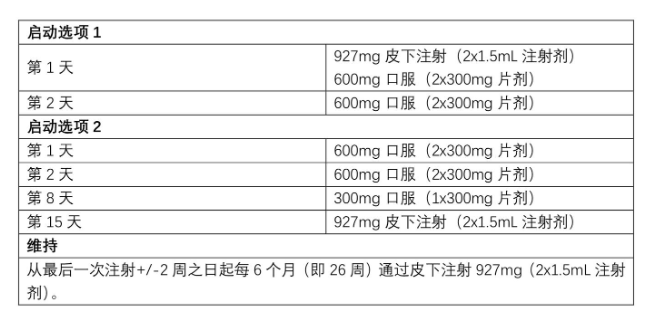
错过剂量:如果自上次注射后超过28周且临床上适合继续使用Sunlenca,则使用选项1或选项2从第1天重新开始。
完整剂量需要两次1.5 mL 皮下注射。
【注意事项】
免疫重建综合征:可能需要进一步评估和治疗。
lenacapavir的残留浓度可能会在体循环中保留长达12个月或更长时间。就给药方案向患者提供建议;不依从性可能导致病毒学应答丧失和耐药性的进展。
在来那帕韦(Lenacapavir)Sunlenca最后一次皮下给药后9个月内开始,可能会增加对主要由CYP3A代谢的药物的暴露和不良反应的风险。
如果停药,尽可能在最后一次注射来那帕韦(Lenacapavir)Sunlenca后28周内启动替代的、完全抑制性抗逆转录病毒治疗方案。如果发生病毒学失败,请尽可能改用替代方案。
可能会发生注射部位反应,结节和硬结可能会持续存在。

作为印度最大的生物制药公司,仿制药巨头太阳制药(Sun Pharma)通过收购女性健康领域的领军企业Organon,实现了规模翻番。凭借这笔117.5亿美元的交...
随着诺和诺德旗下热门糖尿病和肥胖症药物 Ozempic 与 Wegovy 在印度的专利于今日到期,预计将有超过 40 家仿制药企业开始在该国推出各自的低价版本。...

随着诺和诺德近期推出 Wegovy 口服片,打开了 GLP-1 口服药在肥胖症领域的市场,该公司如今又公布了积极结果,有望将司美格鲁肽的适应症扩展至其最初获批的...

中国已成为首个批准罗氏旗下阵发性睡眠性血红蛋白尿症(PNH)药物可伐利单抗(crovalimab)的国家。该药是阿斯利康输注制剂 Soliris 和 Ultom...

得益于长效抗逆转录病毒疗法Cabenuva的增长,葛兰素史克(GSK)对其整体HIV业务提出了更为乐观的展望。GSK旗下专业HIV公司ViiV Healthca...
在 Soliris 获得 FDA 批准用于治疗视神经脊髓炎谱系疾病(NMOSD)近五年后,阿斯利康的下一代 C5 药物 Ultomiris 也成功进入了这一罕见...






