对于慢性免疫性血小板减少症(ITP)的患者而言,血小板计数的“跌跌撞撞”时刻牵动着心弦。当病程超过一年,进入慢性阶段,寻找一种能长期、稳定、安全提升血小板的治疗方案,成为无数患者和家属最深切的渴望。今天,我们要认识的艾曲波帕,正是这样一款改变了ITP治疗格局的口服靶向药物。它如何工作?长期使用效果和安全性如何?更重要的是,面对长期治疗的经济压力,我们是否有更明智的选择?本文将抽丝剥茧,提供一份全面的“长期用药指南”。
升板新机制:艾曲波帕如何“制造”血小板?
血小板减少症我们可以简单的理解成是生产血小板的“工厂”出了问题,要想解决这个问题就要从“生产线”入手。艾曲波帕作为血小板生成素受体激动剂(TPO-RA)可以作用于巨核细胞表面的TPO受体,也就是摇身一变成为了工厂里面的“生产队长”,发出“加速生产”的信号,进而促进血小板快速、大量的生成。
疗效深解读:长期研究证实了哪些硬核实力?
艾曲波帕不仅短期效果显著,在年复一年的慢性ITP治疗中也能保持稳定发挥。
快速且持续升板:治疗第2周,患者的中位血小板计数就升至安全水平(≥50×10⁹/L),并且在此安全水平内维持5年以上。
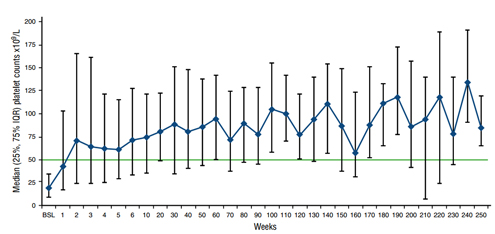
这意味着艾曲波帕不仅有利于血小板减少症的快速治疗,更有利于长期维持。
总体反应率高:87%的患者在无需紧急干预的情况下,血小板至少一次达标。
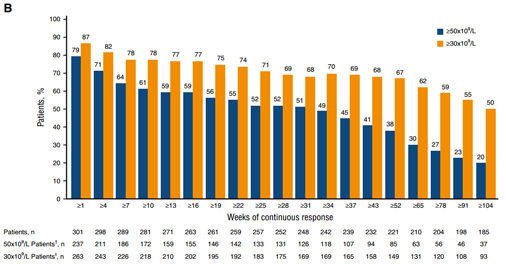
表明大多数患者仅治疗一周,血小板水平就已达标。
显著减少出血风险:患者经过一年的治疗,出血发生率降低了近一半(41%)。
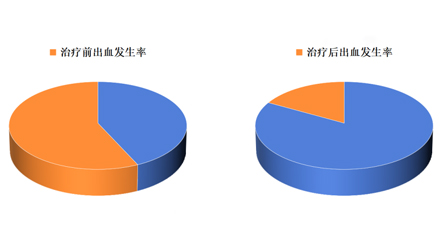
患者使用艾曲波帕治疗后出血风险大幅降低,生活质量得到有效保障。
安全与剂量:长期服用的“护身符”与“方向盘
任何长期用药,安全性和剂量管理都是重中之重。艾曲波帕在使用过程中除了需关注头痛、鼻咽炎这类常见的不良反应,以及定期监测血栓风险和肝功能指标外,还应重点关注使用剂量的问题。研究显示高达95%的患者在长期治疗的过程中需要调整剂量,以便于将血小板的数量维持在理想区间(通常为50-150×10⁹/L)。
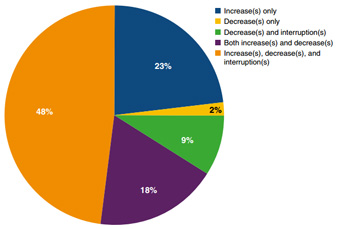
因此,患者在选用艾曲波帕进行治疗期间,需定期监测血小板水平并及时与医生沟通,根据自身实际情况调整用药剂量。找到“最小有效剂量”,这既能保证疗效,又能最大程度降低潜在风险和费用。
从原研到仿制:同样的疗效,更可及的未来
了解了艾曲波帕优异的长期疗效和可控的管理策略后,一个现实而又紧迫的问题出现在眼前:那么贵!怎么买?原研药的价格对于需要数年甚至更长期服用的患者家庭来说,是一笔巨大的持续性花销。患者根本买不起,就算买起也很难负担长期治疗的费用。此时,艾曲波帕仿制药的出现,为长期治疗带来了“疗效不减,负担大减”的可能性。
仿制药真的靠谱吗?答案是肯定的。正规的仿制药与原研药在有效成分、剂量、作用机制和生物等效性上完全一致。它们都经过药监部门的严格审批,确保其安全性和有效性达到同等标准。
为何要考虑仿制药?
疗效保证:核心治疗成分完全相同,确保升板效果。
经济减压:价格通常仅为原研药的几分之一,极大降低长期治疗的经济门槛。
提升治疗依从性:费用压力减轻后,患者更能坚持服药和定期复查,为长期治疗打下基础。
市场选择指南:主流艾曲波帕仿制药厂家一览
目前,全球多个信誉良好的制药企业生产了高质量的艾曲波帕仿制药,为患者提供了多样化的选择。以下是部分主流产品信息,仅供参考:
孟加拉版仿制药是备受认可的国际市场主流,珠峰制药(Everest)、耀品国际(DrugInternational)、BEACON等厂家规格为50mg*28粒/盒或25mg*28粒/盒的的仿制药价格普遍在500-1000元之间。
老挝版的仿制药是性价比突出的后起之秀,卢修斯制药(Lucius)和东盟制药(T.L.Pharma)等厂家的仿制药价格在600-700元不等。
艾曲波帕为慢性ITP的长期管理提供了强效、可靠的新选择。而高质量仿制药的出现,让这一先进疗法变得更加触手可及。希望这篇文章能帮助在抗击ITP的漫长道路上的患者及其家属,掌握更多信息,做出更从容、更经济的决策,稳稳地提升生命的“板值”。
本文数据及图片来源:Wong, Raymond S M et al. “Safety and efficacy of long-term treatment of chronic/persistent ITP with eltrombopag: final results of the EXTEND study.” Blood vol. 130,23 (2017): 2527-2536. doi:10.1182/blood-2017-04-748707