创新药物获批:抗疫战线再添国产利器
11月5日,国家药品监督管理局通过附条件批准程序,正式批准浙江艾森药业有限公司申报的1类创新药奥格特韦钠胶囊上市。该药物作为口服小分子新冠病毒感染治疗药物,适用于治疗轻中型新型冠状病毒感染(COVID-19)的成年患者,标志着我国在新冠治疗药物研发领域取得重要突破。
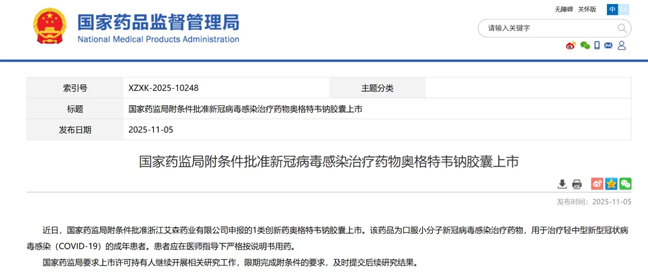
奥格特韦钠胶囊的获批,为我国疫情防控体系再添重要工具。在全球新冠疫情持续演变的背景下,这款国产创新药的成功上市,不仅丰富了临床治疗选择,更展现了我国医药企业的研发实力和创新水平,为构建更加完善的新冠治疗体系提供了有力支撑。
药物特性解析:小分子药物的治疗优势
作为口服小分子药物,奥格特韦钠胶囊具有独特的药学优势。小分子药物通常具有更好的组织渗透性和生物利用度,能够更有效地作用于病毒复制关键靶点。与生物大分子药物相比,口服给药方式更为便捷,可显著提升患者用药依从性,降低医疗资源占用。
该药物的附条件批准上市,是基于其临床研究数据显示出良好的安全性和有效性。在临床试验中,奥格特韦钠胶囊针对轻中型新冠肺炎成年患者展现出显著的治疗效果,能够有效缓解临床症状、缩短病程,并降低疾病进展风险,为患者提供了新的治疗选择。
临床价值凸显:完善疫情防控体系
奥格特韦钠胶囊的上市,进一步完善了我国新冠肺炎分级诊疗体系。对于轻中型患者而言,早期有效的抗病毒治疗至关重要,能够有效防止病情向重症发展,减轻医疗系统压力。这款口服药物的便捷性特点,使其特别适合在基层医疗机构推广应用。
业内专家表示,在疫情防控常态化的背景下,奥格特韦钠胶囊的获批具有重要战略意义。它不仅为临床医生提供了新的治疗武器,更重要的是展现了我国创新药研发能力的持续提升。随着更多创新药物的涌现,我国在应对新发突发传染病方面的药物储备将更加充实。
发展前景展望:创新研发持续推进
奥格特韦钠胶囊的成功上市,是浙江艾森药业研发实力的重要体现。作为1类创新药,该产品从研发到获批的全过程,都彰显了我国药品审评审批制度改革取得的成效。附条件批准政策的实施,使得具有突出临床价值的创新药能够更快惠及患者。
未来,随着更多临床数据的积累和真实世界研究的开展,奥格特韦钠胶囊有望在新冠治疗领域发挥更大作用。同时,该药物的研发经验也将为我国创新药企业发展提供重要借鉴,推动整个行业向更高水平迈进。在全球医药创新竞争日益激烈的背景下,此类突破性产品的出现,预示着中国制药创新正迎来新的发展机遇。