北京协和医学院王金华教授团队发表最新研究成果,首次揭示γ-干扰素诱导溶酶体硫醇还原酶(IFI30)在乳腺癌免疫抑制微环境形成中的关键作用。该研究不仅阐明了IFI30通过双重机制促进乳腺癌进展的内在机理,更为破解乳腺癌免疫治疗耐药难题提供了新的靶点方向。
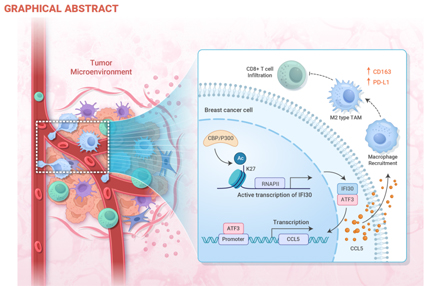
突破性发现:IFI30成乳腺癌免疫治疗新靶点
研究团队通过分析临床样本发现,IFI30在乳腺癌组织及患者血清中均显著高表达,且与患者不良预后密切相关。机制研究表明,这一异常表达源于乳腺癌细胞中H3K27ac修饰在IFI30启动子区域的异常富集。尤为关键的是,研究证实IFI30通过泛素-蛋白酶体途径降解,其稳定性直接影响肿瘤进展。
研究团队通过构建免疫正常和免疫缺陷小鼠模型进行对比实验,发现IFI30对肿瘤生长的促进作用完全依赖于功能性免疫系统。这一发现将研究焦点引向了肿瘤免疫微环境,为后续机制探索指明了方向。
双重机制:IFI30如何塑造免疫抑制微环境
深入研究表明,IFI30通过双重机制协调乳腺癌免疫抑制微环境。在癌细胞层面,IFI30与转录因子ATF3相互作用,激活CCL5趋化因子的转录与分泌,从而促进肿瘤相关巨噬细胞(TAMs)向肿瘤部位的募集。
在免疫细胞层面,乳腺癌细胞通过分泌细胞因子诱导TAMs中IFI30的表达上调,进而驱动巨噬细胞向M2型极化,并显著提升PD-L1的表达水平。这种双向调控机制共同构建了有利于肿瘤生长的免疫抑制环境。
临床价值:为联合治疗提供新思路
该研究的临床价值在于揭示了同时靶向癌细胞和免疫细胞中IFI30的治疗潜力。在自发乳腺癌模型中,IFI30基因缺失不仅延迟了肿瘤发生、抑制了转移,还显著延长了小鼠的生存期。单细胞测序和空间转录组学分析进一步证实,IFI30缺陷肿瘤中TAMs浸润减少,同时CD8+T细胞积聚增强。
值得注意的是,研究团队发现IFI30在多种肿瘤类型中与免疫检查点分子及MHC基因表达呈强相关性,提示其可能成为预测免疫治疗疗效的生物标志物。这些发现为开发针对IFI30的靶向药物,以及将其与现有免疫检查点抑制剂联合使用提供了理论依据。
王金华教授表示:“这项研究揭示了IFI30在协调肿瘤免疫微环境中的核心作用,针对这一靶点的治疗策略有望克服当前乳腺癌免疫治疗的局限性”。
该研究获得国家自然科学基金重点项目支持,相关专利已进入实质审查阶段。业内专家认为,这一发现不仅为乳腺癌治疗开辟了新路径,也为实体肿瘤免疫治疗研究提供了重要参考。