处方药 印度
| 通用名称 | 飞尼妥、Everolimus、Afinitor |
| 药品规格 | 5mg*10片 10mg*10片 |
| 生产企业 | 印度格伦马克Glenmark制药 |
| 功能主治 | (1)既往接受舒尼替尼或索拉非尼治疗失败的晚期肾细胞癌成人患者。 (2)不可切除的、局部晚期或转移性的、分化良好的(中度分化或高度分化)进展期胰腺神经内分泌瘤成人患者。 (3)需要治疗干预但不适于手术切除的结节性硬化症(TSC)相关的室管膜下巨细胞星形细胞瘤(SEGA)成人和儿童患者 |
注:依维莫司(Everolimus) 为处方药物,外包装仅供参考,需在医生指导下使用,用药前请仔细阅读药品说明书,了解用法用量、禁忌症及不良反应。
【药品说明书】
(1)既往接受舒尼替尼或索拉非尼治疗失败的晚期肾细胞癌成人患者。
(2)不可切除的、局部晚期或转移性的、分化良好的(中度分化或高度分化)进展期胰腺神经内分泌瘤成人患者。
(3)需要治疗干预但不适于手术切除的结节性硬化症(TSC)相关的室管膜下巨细胞星形细胞瘤(SEGA)成人和儿童患者
应由有肿瘤或结节性硬化症治疗经验的医生指导下使用本品进行治疗。
晚期肾细胞癌和晚期胰腺神经内分泌瘤
依维莫司推荐剂量:
本品的推荐剂量为10mg每日一次。
本品每日一次口服给药,在每天同一时间服用,可与食物同服或不与食物同时服用。
非感染性肺炎,感染,口腔溃疡,肾功能衰竭。
30℃以下贮藏。避光、防潮。避免儿童误取。
(1)既往接受舒尼替尼或索拉非尼治疗失败的晚期肾细胞癌成人患者。 (2)不可切除的、局部晚期或转移性的、分化良好的(中度分化或高度分化)进展期胰腺神经内分泌瘤成人患者。 (3)需要治疗干预但不适于手术切除的结节性硬化症(TSC)相关的室管膜下巨细胞星形细胞 瘤(SEGA)成人和儿童患者
1.强CYP3A4抑制剂:避免同时使用。
2.中度CYP3A4和/或PgP抑制剂:如需要联用,谨慎使用和减低AFINITOR剂量。
3.强CYP3A4诱导剂:避免同时使用。
如不能避免联用,增加AFINITOR的剂量
24个月
片剂
印度Glenmark
依维莫司。化学名:40-O-(2-羟乙基)-雷帕霉素分子量:C53H83NO14
白色或微黄色片
1.非感染性肺炎:监查临床症状或放射学变化;曾发生致命性病例。
通过减低剂量或停药处理直至症状解决,和考虑使用皮质甾体。
2.感染:增加感染的风险,有些致命性。
监视征象和症状,和及时治疗。
3.口腔溃疡:口溃疡,口炎,和口粘膜炎是常见的。
处理包括口腔洗涤(无酒精或过氧化物)和局部治疗。
4.实验室检验改变:可能发生血清肌酐,血糖,和脂质的升高。
还可能发生血红蛋白,嗜中性,和血小板减低。
治疗前和以后定期监测肾功能,血糖,脂质,和血液学参数。
5.免疫接种:避免活疫苗和密切接触曾接受活疫苗者。
6.妊娠中使用:当给予妊娠妇女时可能发生胎儿危害。
告知妇女对胎儿潜在危害。
【适应症】
(1)既往接受舒尼替尼或索拉非尼治疗失败的晚期肾细胞癌成人患者。
(2)不可切除的、局部晚期或转移性的、分化良好的(中度分化或高度分化)进展期胰腺神经内分泌瘤成人患者。
(3)需要治疗干预但不适于手术切除的结节性硬化症(TSC)相关的室管膜下巨细胞星形细胞瘤(SEGA)成人和儿童患者
【副作用】
非感染性肺炎,感染,口腔溃疡,肾功能衰竭。
【用法用量】
应由有肿瘤或结节性硬化症治疗经验的医生指导下使用本品进行治疗。
晚期肾细胞癌和晚期胰腺神经内分泌瘤
依维莫司推荐剂量:
本品的推荐剂量为10mg每日一次。
本品每日一次口服给药,在每天同一时间服用,可与食物同服或不与食物同时服用。
【注意事项】
1.非感染性肺炎:监查临床症状或放射学变化;曾发生致命性病例。
通过减低剂量或停药处理直至症状解决,和考虑使用皮质甾体。
2.感染:增加感染的风险,有些致命性。
监视征象和症状,和及时治疗。
3.口腔溃疡:口溃疡,口炎,和口粘膜炎是常见的。
处理包括口腔洗涤(无酒精或过氧化物)和局部治疗。
4.实验室检验改变:可能发生血清肌酐,血糖,和脂质的升高。
还可能发生血红蛋白,嗜中性,和血小板减低。
治疗前和以后定期监测肾功能,血糖,脂质,和血液学参数。
5.免疫接种:避免活疫苗和密切接触曾接受活疫苗者。
6.妊娠中使用:当给予妊娠妇女时可能发生胎儿危害。
告知妇女对胎儿潜在危害。
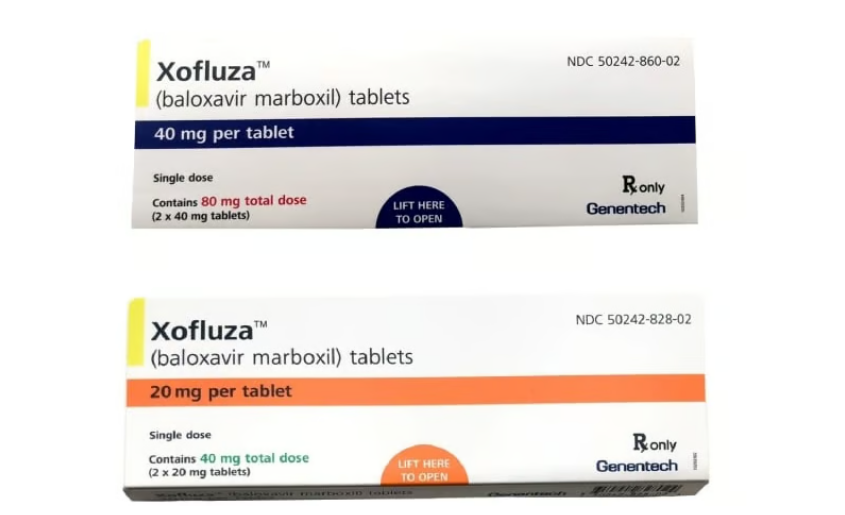
罗氏已签署一项自愿许可协议,允许仿制药企在129个发展中国家复制其畅销流感抗病毒药物Xofluza(巴洛沙韦马布酯)。药品专利池(MPP)在5月18日发布的公告...

去年秋天 III 期临床数据亮眼之后,阿斯利康对 CinCor Pharma 及其醛固酮合酶抑制剂(ASI)baxdrostat 的押注持续获得回报。FDA 已...
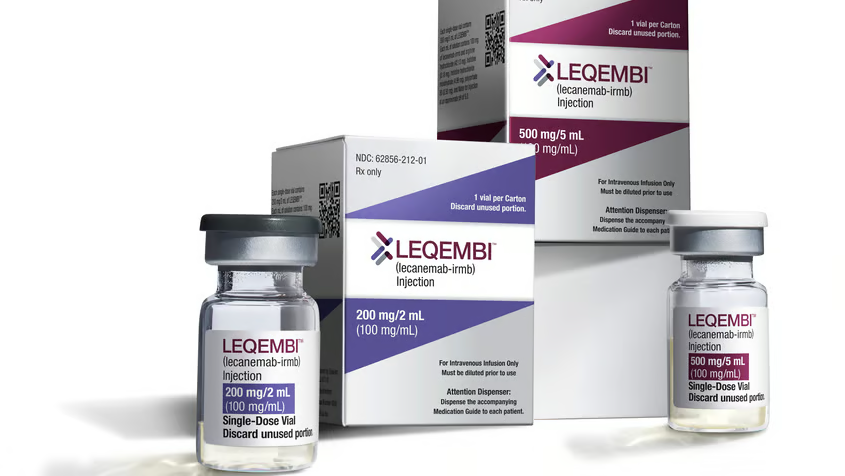
如今,卫材在 5 月 15 日发布的全年财报演示中表示,预计 2026 财年 Leqembi 的收入将达到 1435 亿日元(约合 9.046 亿美元)。大部分...

仿制药巨头太阳制药(Sun Pharma)正在美国召回一批化疗药物,颗粒物污染问题再次出现在 FDA 的召回名单上。 根据 FDA 网站上发布的公告,太阳制药此...

在抗癌免疫疗法Unloxcyt获得FDA批准三个月后,Checkpoint Therapeutics找到了买家。 两家公司周日宣布,太阳制药已同意以3.55亿美...
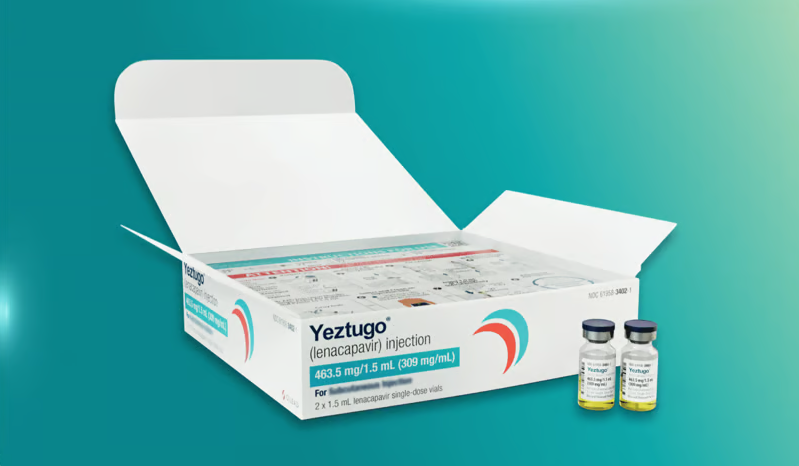
从长达17年的研发周期到最终商业化上市,生产一直深深植根于Yeztugo的DNA之中。对于这款每年只需注射两次的暴露前预防(PrEP)药物——吉利德科学将其定位...






